La evaporación ocurre cuando un líquido se convierte en gas. ¿Alguna vez has notado que cuando se deja un vaso sobre la encimera, el agua comienza a evaporarse? Es evaporación, no hadas sedientas que habitan en tu cocina. La evaporación es el proceso mediante el cual las moléculas experimentan una transición espontánea de la fase líquida a la fase gaseosa. La evaporación es lo opuesto a la condensación.
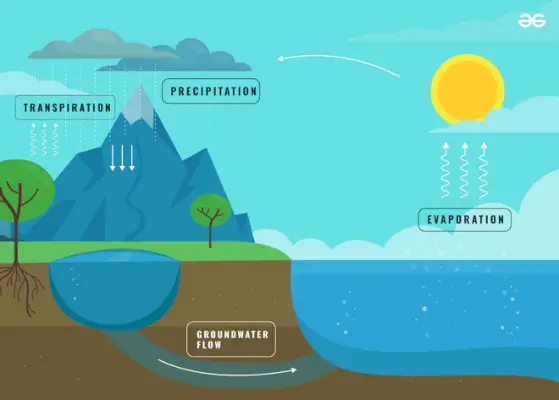
Evaporación
Un tipo de vaporización llamado evaporación implica la transferencia de partículas líquidas a la fase gaseosa y normalmente tiene lugar en la superficie de los líquidos. En consecuencia, se afirma que este proceso implica un cambio en el estado de la materia de los líquidos.
Tabla de contenidos
- ¿Qué es la evaporación?
- Ejemplos de evaporación
- Proceso de evaporación
- Factor que afecta la evaporación
- Diferencia entre evaporación y ebullición
- Diferencia entre evaporación y vaporización
¿Qué es la evaporación?
La evaporación es un proceso en el que el estado líquido de la materia se convierte en un estado gaseoso en presencia de calor.
Mucha gente confunde entre evaporación y ebullición, ya que al hervir, el líquido también cambia a estado gaseoso. Pero hay una diferencia. La primera es que la ebullición del líquido ocurre a una temperatura particular, mientras que la evaporación puede ocurrir a cualquier temperatura por debajo del punto de ebullición. Además, la ebullición es un fenómeno de masa, mientras que la evaporación es un fenómeno de superficie, lo que significa que la evaporación sólo puede ocurrir en la superficie del líquido.

Durante la evaporación, la molécula que tenía mayor energía cinética solo se disipó de la capa superior del líquido. También hay una propiedad única de la evaporación que provoca un efecto refrescante. La vasija de barro se usaba para almacenar agua fría en verano, ya que el agua se filtraba por los pequeños poros de la vasija, provocando la evaporación y provocando el enfriamiento del agua dentro de la vasija. El enfriador del desierto también funciona según el principio de evaporación.
Para que se produzca la evaporación, las moléculas de un líquido deben estar cerca de la superficie, deben alejarse del cuerpo del líquido y deben tener suficiente energía cinética para escapar de la interfaz. Cuando las moléculas escapan, la energía cinética promedio de las moléculas restantes disminuye. Esto reduce la temperatura del líquido y es la base del fenómeno del enfriamiento por evaporación.
La evaporación también depende de algunos factores, como la temperatura, la superficie del líquido, la velocidad del viento y la humedad. Discutiremos esto en detalle en este artículo.
Ejemplos de evaporación
Hay muchos ejemplos de evaporación, pero aquí discutiremos solo algunos de ellos:
- Secado de ropa al sol: Todos secamos nuestra ropa al sol, la ropa mojada se seca debido a la evaporación donde el agua se convierte en vapor de agua.
- Secado de cuerpos de agua: Hemos visto en verano que el agua de los estanques y del lago disminuye o, a veces, se seca debido a la evaporación.
- El ciclo del agua: Este es un muy buen ejemplo de evaporación; en los dos anteriores discutimos cómo la evaporación convierte el agua en vapor de agua. Este vapor de agua sube al cielo y se condensa para formar una nube, y luego precipitó. Entonces, la evaporación es importante para regular el ciclo del agua.
- Formación de sal: De forma natural o industrial la sal se forma debido a la evaporación donde el agua se evapora para dejarnos sal.
- Secado de un piso trapeado
- Trabajar en el desierto más fresco en verano.
Proceso de evaporación
Un líquido se evapora cuando se calienta. Esto implica que las moléculas del líquido deben adquirir energía cinética. Las moléculas de un líquido se expanden y vibran más rápidamente a medida que adquiere energía cinética. Como resultado, el líquido se convierte en gas, cambiando su estado de la materia.
El agua es una sustancia común donde se produce la evaporación. El agua cambia de líquido a gas cuando se aplica energía o calor porque los enlaces que mantienen unidas las moléculas comienzan a debilitarse. El punto de ebullición del agua, que es 212 grados Fahrenheit o 100 grados Celsius, es el punto en el que se transforma de líquido a gas.
Factor que afecta la evaporación
La evaporación facilita nuestra vida de muchas maneras e incluso contribuye al ciclo del agua. Pero la evaporación depende de algunos factores que controlarán la tasa de evaporación. Una cosa más a tener en cuenta: la evaporación es un proceso lento, pero algunos factores externos aumentan o disminuyen la velocidad de evaporación. Analicemos todos estos factores de evaporación:
Temperatura
El primer factor es la temperatura, ya que sabemos que la evaporación puede ocurrir a cualquier temperatura antes del punto de ebullición, pero la temperatura también influye en la evaporación. Determinará la tasa de evaporación, cuanto mayor sea la temperatura, mayor será la tasa de evaporación. Ahora la pregunta es ¿cómo? Todos sabemos que la temperatura aumentará la energía cinética, ya que la energía se utiliza para romper las fuerzas intermoleculares que unen la molécula del líquido. Entonces, cuando aplicamos más temperaturas la molécula rompe rápidamente sus fuerzas intermoleculares y se evapora.
Esto implica,
Temperatura ∝ Evaporación
Por ejemplo, todos hemos visto en el verano caluroso que la ropa se seca más rápidamente que en los días normales. Esto se debe al factor temperatura.
Debe revisar
- Unidad de temperatura
- Relación entre la escala de temperatura Celsius y Kelvin
- Efecto del cambio de temperatura
Área de superficie del líquido
Anteriormente discutimos que la evaporación es un fenómeno superficial y la superficie juega un papel en la tasa de evaporación. Cuanto mayor sea la superficie, mayor será la tasa de evaporación. Entonces, si habrá más área de superficie, entonces se presentarán más moléculas líquidas en la superficie, lo que significa que más moléculas romperán sus enlaces intermoleculares, lo que aumentará la velocidad de evaporación. Entonces podemos escribirlo como;
Área de superficie del líquido ∝ Evaporación
Por ejemplo, la misma cantidad de agua se evapora más rápidamente en un plato que el agua en un vaso poco profundo, esto se debe a que el plato ofrece una mayor superficie para el líquido que el vaso poco profundo.
Humedad
La humedad se refiere a la cantidad de humedad o vapor de agua en el aire . Cuanto más vapor de agua haya en el aire diremos más humedad. A mayor humedad, la tasa de evaporación disminuye.
Humedad ∝ 1/Evaporación
Por ejemplo, en la temporada de lluvias, cuando nuestro entorno es más húmedo, es muy difícil secar la ropa.
Velocidad del viento
La velocidad del viento es directamente proporcional a la evaporación, lo que significa que con el aumento de la velocidad del viento habría un aumento en la tasa de evaporación.
Velocidad del viento ∝ Evaporación
Por ejemplo, en un día ventoso, la ropa se seca más rápido que en días normales. Esto se debe a que el viento disminuyó la humedad, lo que aumentará la tasa de evaporación.
Leer también
- Efectos de la humedad relativa y la velocidad del viento
Diferencia entre evaporación y ebullición
A continuación se muestran las principales diferencias entre evaporación y ebullición.
| Evaporación | Hirviendo |
|---|---|
| La evaporación es un proceso natural en el que el líquido cambia a forma gaseosa debido a un aumento de temperatura, presión o ambas. | La ebullición es simplemente la vaporización, que convierte el líquido en gas mediante calentamiento continuo. |
| La evaporación ocurre sólo en la superficie del líquido. | Sin embargo, la ebullición se produce en toda la gran masa de la sustancia. |
| En caso de evaporación, la temperatura no supera el punto de ebullición del líquido. | Sin embargo, en la ebullición, el proceso ocurre sólo en el punto de ebullición del líquido. |
| Por tanto, es un proceso lento. | Por tanto, este es un proceso rápido. |
| La tasa de evaporación aumenta con un aumento en el área de superficie abierta del líquido. | La velocidad de ebullición es independiente del área de la superficie abierta del líquido. |
Diferencia entre evaporación y vaporización
La diferencia entre evaporación y vaporización se tabula a continuación:
| Evaporación | Vaporización |
|---|---|
| Fenómeno superficial | Fenómeno masivo |
| Ocurre a cualquier temperatura. | Ocurre a una temperatura específica. |
| Ocurre sólo en la superficie de un líquido. | Ocurre en toda la masa del líquido. |
| El proceso es más lento | El proceso es relativamente más rápido. |
| No es fácilmente visible | Visible durante la ebullición |
| El calor requerido para la evaporación es menor. | El calor requerido para la vaporización es mayor. |
| Ejemplos: secar ropa, charcos | Ejemplos: agua hirviendo, formación de vapor. |
Debe leer
- La evaporación causa enfriamiento
- Separación por evaporación
- Cristalización
Evaporación – Preguntas frecuentes
¿Cuál es la diferencia entre evaporación y vaporización?
El cambio de fase de una sustancia o elemento que tiene lugar durante el proceso de ebullición o sublimación se conoce como vaporización. En pocas palabras, la evaporación es una forma de vaporización que tiene lugar principalmente cuando la temperatura está por debajo del punto de ebullición. El estado de una sustancia puede cambiar de sólido o líquido a gas mediante vaporización.
¿Cuáles son los factores que afectan la evaporación?
A continuación se presentan algunos factores que determinan la tasa de evaporación:
- Área de superficie del líquido: Cuanto mayor sea el área de superficie, mayor será la tasa de evaporación. Por tanto, el área de superficie del líquido ∝ evaporación.
- Humedad: A mayor humedad, la tasa de evaporación disminuye, significa Humedad ∝ 1/Evaporación.
- Velocidad del viento: La velocidad del viento es directamente proporcional a la evaporación, lo que significa que con el aumento de la velocidad del viento habría un aumento en la tasa de evaporación.
¿En qué se diferencia la evaporación de la ebullición?
El proceso de evaporación es muy diferente al de ebullición en muchos aspectos. La evaporación es un proceso natural en el que el líquido cambia a forma gaseosa debido a un aumento de temperatura, presión o ambas. Sin embargo, la ebullición no es un proceso natural, es simplemente la vaporización, que convierte el líquido en gas mediante calentamiento continuo.
¿Cómo ocurre la evaporación en el ciclo del agua?
Cuando la luz del sol calienta la superficie del agua, la evaporación tiene lugar como parte del El ciclo del agua . El calor del sol hace que las moléculas de agua viajen cada vez más rápido hasta que puedan escapar en forma de gas. Una molécula de vapor de agua pasa aproximadamente 10 días en la atmósfera después de haberse evaporado.
¿Qué es la evaporación? Dar un ejemplo.
La evaporación es un proceso en el que el estado líquido de la materia se convierte en un estado gaseoso en presencia de calor. Por ejemplo, todos secamos nuestra ropa al sol, la ropa mojada se seca debido a la evaporación donde el agua se convierte en vapor de agua.
¿Por qué es muy difícil secar la ropa en la estación húmeda?
Ya que sabemos que la humedad se refiere a la cantidad de humedad o vapor de agua que hay en el aire. Cuanto más vapor de agua hay en el aire diremos que más es humedad. A mayor humedad, la tasa de evaporación disminuye. Por lo tanto, será muy difícil secar la ropa en la estación húmeda.
Escribe cuatro ejemplos de evaporación.
Ejemplos de evaporación son los siguientes:
java es igual
- Secado de cuerpos de agua.
- El ciclo del agua
- formación de sal
- Secado de un piso trapeado
¿Cómo afecta el aumento de temperatura a la tasa de evaporación?
Cuanto mayor es la temperatura, mayor es la tasa de evaporación. Esto se debe a que la temperatura aumentará la energía cinética y la energía utilizada para romper las fuerzas intermoleculares que unen la molécula del líquido. Entonces, cuando aplicamos más temperatura, la molécula rompe rápidamente sus fuerzas intermoleculares y se evapora.
¿Qué es lo opuesto a la evaporación?
Condensación es lo opuesto a la evaporación. Un tipo de vaporización llamado evaporación implica la transferencia de partículas líquidas a la fase gaseosa y normalmente tiene lugar en la superficie de los líquidos. En consecuencia, se afirma que este proceso implica un cambio en el estado de la materia de los líquidos.
